Uma equipe de pesquisa liderada por David Reverter, cientista da Universidade Autônoma de Barcelona (UAB), identificou os mecanismos moleculares que regulam a divisão celular bacteriana. A descoberta revela como a proteína MraZ se liga ao cluster do gene dcw para controlar este processo. Os resultados da pesquisa foram publicados em comunicações da natureza.
A divisão celular é essencial para todos os organismos e depende da atividade coordenada de muitas proteínas e componentes reguladores. Na maioria das bactérias, as instruções para esse processo são organizadas em um grupo de genes denominado operon dcw. O cluster contém a informação genética necessária para produzir proteínas responsáveis pela divisão celular e construção da parede celular bacteriana.
Como o operon dcw ativa genes de divisão celular
Os genes neste cluster são ativados por proteínas chamadas fatores de transcrição. Essas proteínas se ligam a uma parte específica do DNA chamada promotor, que marca o local onde a transcrição começa. Esse ponto de partida ocorre antes do primeiro códon (unidade básica da informação genética), que marca o início da sequência da proteína.
Um desses fatores de transcrição é o MraZ, que também é o primeiro gene no operon dcw em todas as bactérias. Quando MraZ ativa o operon, os genes dentro do cluster produzem proteínas necessárias para a divisão bacteriana. Desta forma, o MraZ atua como um regulador chave que controla a atividade dos operons que controlam a divisão celular na maioria das espécies bacterianas.
Imagem dos mecanismos moleculares da divisão bacteriana
Uma equipe de pesquisa da UAB liderada por David Reverter, professor titular do Departamento de Bioquímica e Biologia Molecular da UAB e pesquisador do Instituto de Biotecnologia e Biomedicina da UAB (IBB-UAB), revelou o mecanismo detalhado por trás desta regulamentação. A equipe usou métodos avançados de biologia estrutural, incluindo cristalografia de raios X e microscopia crioeletrônica.
Essas técnicas permitiram aos cientistas determinar como o fator de transcrição MraZ se liga ao promotor do operon dcw em bactérias Micoplasma genitalium. Este microrganismo é frequentemente utilizado em pesquisas de laboratório porque possui um genoma extremamente pequeno.
Visão em nível atômico da ligação da proteína MraZ ao DNA
A região promotora do operon dcw contém quatro segmentos repetidos, ou “caixas”, cada um consistindo de seis nucleotídeos. Estas sequências repetitivas de DNA desempenham um papel fundamental na regulação da transcrição.
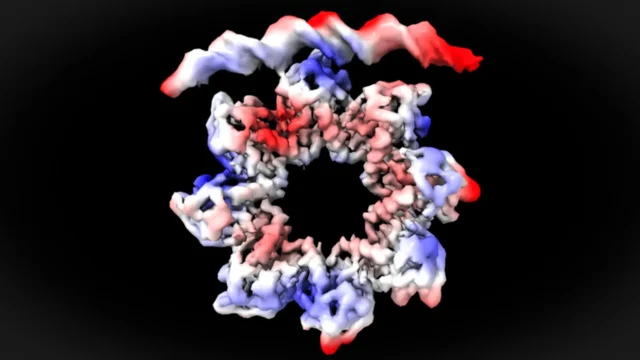
Ao examinar o sistema usando microscopia crioeletrônica, os pesquisadores foram capazes de observar em resolução quase atômica as interações entre a proteína MraZ e as bases de DNA dessas quatro caixas repetidas. Suas observações sugerem que o MraZ deve passar por mudanças estruturais para se ligar com sucesso ao operon.
“Esta foi uma observação surpreendente. A proteína MraZ é um octâmero de oito subunidades idênticas ligadas em forma de donut, mas a sua curvatura nunca permite a ligação às quatro ‘caixas’ do promotor. No entanto, para regular a divisão celular, vemos como o donut se quebra e se deforma para que as quatro subunidades possam juntar-se às quatro caixas do promotor”, explica David Reverter.
Grande avanço na compreensão da divisão celular bacteriana
A observação direta de como o MraZ interage com o DNA promotor que inicia a divisão celular representa um grande avanço. Até agora, os pesquisadores que estudam o sistema basearam-se principalmente em experimentos bioquímicos e modelos computacionais para deduzir como o mecanismo funciona.
Segundo Reverter, o sistema regulatório identificado neste estudo pode estar difundido nas bactérias. “Isso é comum à maioria das bactérias porque todas as proteínas MraZ são muito semelhantes, têm a mesma estrutura de octâmero e sequências de DNA semelhantes nos promotores dos operons que regulam a divisão celular”, concluiu Reverter.
A colaboração internacional por trás da pesquisa
A pesquisa foi liderada pela equipe de David Reverter no Instituto de Biotecnologia e Pesquisa Biomédica da Universidade do Alabama e no Departamento de Bioquímica e Biologia Molecular. Este trabalho foi realizado em colaboração com o Serviço Síncrotron e Cryo-EM da ALBA no Instituto de Genética e Biologia Molecular e Celular de Estrasburgo, França.