O aspecto mais perigoso do cancro não é o tumor original em si, mas a sua capacidade de se espalhar para outras partes do corpo, um processo chamado metástase que é responsável pela maioria das mortes relacionadas com o cancro. A viagem das células cancerígenas desde a sua origem até órgãos distantes envolve transformações complexas que lhes permitem migrar e colonizar novas áreas. Esta transformação é facilitada por um processo que permite que as células cancerígenas alterem as suas características, percam a sua natureza imóvel e ganhem a capacidade de se moverem e invadirem. Compreender esta transição pode ajudar a revelar o comportamento indescritível do cancro e abrir a porta a tratamentos potencialmente inovadores direcionados a estes camaleões celulares.
Uma equipe liderada por Ana-Maria Dragoi, Ph.D., da LSU Health Shreveport, em colaboração com Madison Catalanotto, Camille Abshire, Reneau Youngblood e Min Chu da mesma instituição, Joel Markus Vaz do Georgia Institute of Technology, e o professor Herbert Levine da Northeastern University e Mohit Kumar Jolly, Ph.D., do Indian Institute of Science, alcançaram um grande avanço na compreensão da propagação do câncer. Eles descobriram o importante papel de uma proteína chamada FLASH no processo de transformação conhecido como transição epitelial-mesenquimal (EMT), que controla a propagação das células cancerígenas.
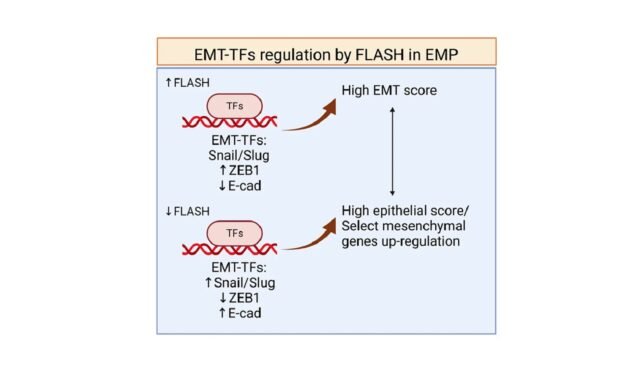
Este processo é crucial para que as células cancerígenas se separem do tumor original e se espalhem para outras partes do corpo. As descobertas da equipe, publicadas na revista Translational Oncology, mostram como a falta de FLASH pode fazer com que as células cancerosas exibam características mistas, nas quais características comportamentais não invasivas coexistem com características invasivas. Ana-Maria Dragoi destacou esta descoberta central: “Primeiro, descobrimos que o FLASH controla a quiescência epitelial das células cancerígenas. Agora sabemos que esta regulação é mais complexa, e o FLASH controla múltiplos aspectos da transformação das células cancerígenas”, observando o seu papel fundamental na progressão e propagação do cancro. Curiosamente, o FLASH aumenta transitoriamente em todas as células à medida que o ciclo celular avança e desempenha um papel fundamental na produção de proteínas de suporte que envolvem o DNA (histonas).
Ao utilizar sequenciamento avançado de RNA e análises computacionais, a equipe identificou o papel único do FLASH na supressão de marcadores de células quiescentes e na afetação de genes associados ao movimento celular. Eles examinaram dados da Cancer Cell Line Encyclopedia (CCLE) para confirmar a relação inversa entre a expressão FLASH e marcadores fenotípicos epiteliais celulares em diferentes tipos de câncer. Consistente com os dados de sequenciamento de RNA, o FLASH também foi inversamente associado a marcadores de transformação de células cancerígenas em certos tipos de câncer. Dr. Dragoi acrescentou: “Demonstramos uma relação inversa entre a expressão FLASH e os marcadores de agressividade do câncer e o comportamento inativo do câncer, no entanto, quando as células cancerígenas não têm FLASH, elas são menos agressivas em geral”. Estes resultados intrigantes demonstram que o FLASH desempenha um papel duplo complexo na regulação do destino celular e conectam-se com dados anteriores que sugerem que as células cancerígenas mais agressivas têm características mistas.
Esta abordagem permite um exame detalhado dos comportamentos genéticos e moleculares que impulsionam o comportamento das células cancerígenas, tornando a ciência acessível a um público amplo e abrindo caminho para estratégias inovadoras de tratamento do cancro. Compreender como o FLASH controla o processo de transformação celular pode levar a novos tratamentos, aumentando a esperança de tratamentos contra o cancro mais eficazes no futuro. Dr. Dragoi enfatizou: “Essas descobertas destacam a importância do FLASH na adaptação e sobrevivência do câncer, tornando-o um alvo promissor para tratamentos futuros”. Este estudo representa um passo importante na nossa compreensão da biologia do câncer e introduz uma nova direção no desenvolvimento de terapias direcionadas ao câncer.
Referência do diário
Madison Catalanotto, Joel Markus Vaz, Camille Abshire, Reneau Youngblood, Min Chu, Herbert Levine, Mohit Kumar Jolly, Ana-Maria Dragoi, “Duplos papéis de CASP8AP2/FLASH na regulação da plasticidade de transição epitelial-mesenquimal (EMP)”, Oncologia Translacional, 2024. DOI: https://doi.org/10.1016/j.tranon.2023.101837.
Sobre o autor
Dra. Anna-Maria Dragoy é professor assistente do Departamento de Fisiologia da LSU Health Shreveport. O seu laboratório estuda a regulação da transição epitelial-mesenquimal no contexto da progressão do ciclo celular e os factores intrínsecos e extrínsecos que regulam a metástase do cancro no contexto da reprogramação oncogénica. Dr. Dragoi é membro da Associação Americana para Pesquisa do Câncer e da Sociedade Americana de Microbiologia.

Dr. Mohit Kumar Jolly é professor associado do Departamento de Bioengenharia do Instituto Indiano de Ciência. Sua pesquisa integra abordagens de biologia de sistemas e abordagens experimentais para elucidar os fatores moleculares da metástase do câncer e da resistência à terapia do câncer. Dr. Jolly é o editor-chefe da NPJ Systems Biology & Applications. Ele é o vencedor da Medalha Jovem Cientista INSA 2022 e do Prêmio ICTP 2023.

Dr. Distinto Professor do Departamento de Física e Engenharia Biológica da Northeastern University. Sua pesquisa se concentra na modelagem computacional e física da plasticidade da transição epitelial-mesenquimal, na regulação genética do destino celular e nas interações entre tumores e o sistema imunológico. Dr. Levine é membro da Academia Americana de Artes e Ciências e da Academia Nacional de Ciências, e co-diretor do NSF Center for Theoretical Biophysics (CTBP) na Rice University.