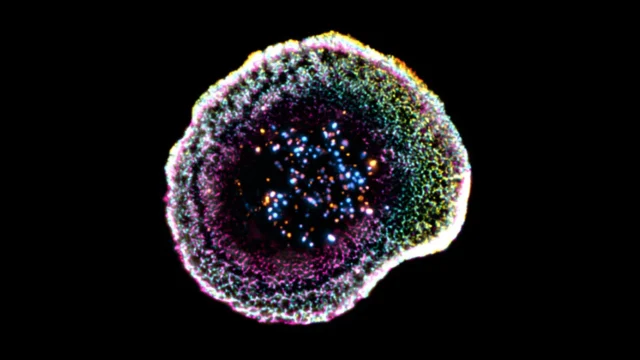
Os linfócitos T citotóxicos atuam como células “assassinas” especializadas do sistema imunológico, procurando e destruindo células infectadas ou cancerosas com altíssima precisão. Sua eficácia depende de um ponto de contato rigidamente controlado chamado “sinapse imunológica”, onde liberam moléculas tóxicas que danificam seus alvos, deixando ilesas as células saudáveis circundantes. Até recentemente, os cientistas lutavam para observar detalhadamente a estrutura fina desse processo. Agora, investigadores da Universidade de Genebra (UNIGE) e do Hospital Universitário de Lausanne (CHUV) conseguiram visualizar estes mecanismos em três dimensões sob condições quase naturais. Suas descobertas foram publicadas em relatório de célulafornece novas pistas sobre como a organização interna das células T citotóxicas apoia a sua função e pode avançar na investigação imuno-oncológica.
Quando o corpo enfrenta uma infecção ou câncer, os linfócitos T citotóxicos ligam-se firmemente aos seus alvos e formam uma sinapse imunológica. Através desta interface especializada, libertam substâncias tóxicas que desencadeiam a destruição de células nocivas. Esta abordagem direcionada permite que o sistema imunológico elimine ameaças de forma eficaz, ao mesmo tempo que minimiza os danos colaterais aos tecidos próximos.
Embora os cientistas já compreendam há muito tempo os fundamentos deste processo, estudar a estrutura detalhada em nanoescala dentro de células humanas intactas continua a ser um desafio. A principal dificuldade surge na forma como as amostras são preparadas, pois os métodos tradicionais podem distorcer delicados componentes celulares. As técnicas de imagem existentes muitas vezes forçam os pesquisadores a escolher entre alta resolução, grandes campos de visão ou preservar a estrutura natural das células.
Microscopia de crioexpansão revela detalhes ocultos
Para superar estes desafios, as equipas UNIGE e CHUV-UNIL, com o apoio do programa TANDEM da Fundação ISREC, utilizaram um método avançado denominado microscopia de crio-expansão (cryo-ExM). Virginie Hamel, professora sênior do Departamento de Biologia Molecular e Celular da Faculdade de Ciências da UNIGE, explica: “Esta técnica envolve o congelamento instantâneo das células em velocidades muito altas, colocando-as no chamado estado vítreo, no qual a água se solidifica sem formar cristais, preservando assim fielmente a estrutura biológica.
Usando esta abordagem, os investigadores descobriram novas características estruturais no ponto onde as células imunitárias atingem os seus alvos. “Nosso trabalho mostra que no ponto de contato entre uma célula imunológica e seu alvo, a membrana forma uma espécie de cúpula, cuja estrutura parece estar relacionada às interações adesivas e à organização interna da célula”, disse Florent Lemaître, pesquisador de pós-doutorado no Departamento de Biologia Molecular e Celular da Faculdade de Ciências da UNGE e primeiro autor do estudo. A equipe de pesquisa também examinou as partículas citotóxicas responsáveis por matar as células-alvo com uma clareza sem precedentes. Eles descobriram que as estruturas dessas partículas podem variar, às vezes contendo um ou mais “núcleos” nos quais as moléculas ativas estão concentradas.
De células de laboratório a tumores reais
Os pesquisadores expandiram seu método além das células isoladas e aplicaram-no diretamente em amostras de tumores humanos. “Estendemos esta abordagem ao tecido tumoral humano, tornando possível observar diretamente os linfócitos T que se infiltram no tumor e os seus mecanismos citotóxicos à nanoescala. Isto permitiu-nos estudar a resposta imunitária diretamente num ambiente clínico e compreender melhor os mecanismos que determinam a sua eficácia”, explica Benita Wolf, residente-chefe e investigadora associada da Divisão de Oncologia Clínica do CHUV, que co-liderou o estudo.
Ao fornecer uma visão tridimensional e quase nativa de como essas células imunológicas operam, este trabalho fornece uma estrutura valiosa para o estudo das respostas imunológicas em condições do mundo real. Estas informações podem ajudar-nos a melhorar os tratamentos, particularmente em imuno-oncologia, melhorando a nossa compreensão dos factores e limitações do ataque imunitário bem sucedido contra o cancro.