O linfoma anaplásico de grandes células (ALCL) é um linfoma agressivo de células T CD30+ que representa um enorme desafio para a oncologia devido à sua base genética complexa e à resistência às terapias convencionais. Pesquisadores liderados pelo professor Thomas Look, do Dana-Farber Cancer Institute e do Boston Children’s Hospital, elucidaram um mecanismo-chave da patologia ALCL, fornecendo caminhos potenciais para terapia direcionada. Suas descobertas, publicadas na Cell Reports Medicine, revelam como a principal proteína sinalizadora STAT3 se integra aos principais reguladores transcricionais para manter o estado maligno do ALCL.
Uma equipe de pesquisadores, incluindo Nicole Prutsch, Ph.D., Brian Abraham, Ph.D., Mark Zimmerman, Ph.D., e colegas iniciaram o estudo para compreender o papel preciso do STAT3 no ALCL. Sua colaboração inclui instituições como o Hospital de Pesquisa Infantil St. Jude, a Universidade de Cambridge, a Universidade Médica de Viena e o Instituto do Câncer Dana-Farber. O estudo foi publicado na revista Cell Reporting Medicine, revisada por pares.
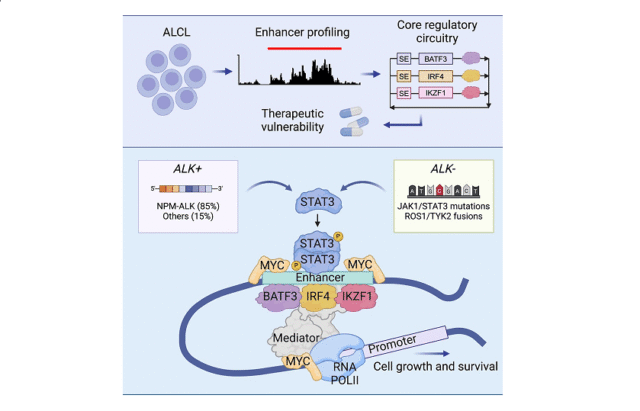
ALCL é frequentemente impulsionado por rearranjos cromossômicos que ativam a tirosina quinase ALK ou outras mutações que resultam na ativação sustentada da via de sinalização JAK-STAT. O professor Look e sua equipe descobriram que nas células ALCL, o STAT3 ativado combina-se com outros fatores-chave de transcrição (BATF3, IRF4 e IKZF1) para formar um circuito regulador central (CRC) que promove a sobrevivência e proliferação das células cancerígenas. “Nosso estudo mostra que as células ALCL são altamente dependentes de um pequeno grupo central de fatores regulatórios de transcrição. Visar essas dependências abre novos caminhos para intervenção terapêutica”, disse o Dr. Zimmerman.
A equipe usou o sequenciamento de imunoprecipitação da cromatina (ChIP-seq) para mapear regiões intensificadoras em células ALCL e identificou um conjunto de superintensificadores conservados relacionados a genes como BATF3, IRF4 e IKZF1. Estas regiões são altamente enriquecidas para H3K27ac, uma modificação de histonas característica de potenciadores activos, sublinhando o papel dos factores de transcrição codificados por estes genes na condução da expressão de alto nível de programas genéticos expandidos críticos para o fenótipo maligno. Além disso, a análise de ocupação genómica demonstrou que o STAT3, após activação pela ALK quinase, coopera com super-intensificadores destes factores de transcrição CRC para assegurar a expressão sustentada de oncogenes.
Este estudo destaca que o STAT3, embora não atenda aos critérios canônicos para um componente CRC devido à falta de um superintensificador para conduzir sua expressão, desempenha um papel fundamental como fator de transcrição responsivo ao sinal. Uma vez ativado pela sinalização da tirosina quinase, o STAT3 coopera com o CRC para regular a expressão do conhecido oncogene MYC. “Nossos resultados indicam que o STAT3, juntamente com os fatores de transcrição do CRC, impulsiona um programa de expressão oncogênica no ALCL”, observou o Dr. Abraham.
O professor Look enfatizou o significado de longo prazo de sua pesquisa, dizendo: “A descoberta do meu laboratório em 1994 do gene ALK e do gene de fusão NPM-ALK, que fornece um sinal ativador de tirosina quinase que ativa STAT3, fornece um mecanismo de transformação chave para a maioria dos ALCL que abrigam a translocação cromossômica t (2; 5), como nosso estudo relatou no artigo atual, 30 anos depois, destaca. “
Em ensaios funcionais, os pesquisadores demonstraram que a interrupção de qualquer componente do CRC prejudicou significativamente o crescimento e a viabilidade das células ALCL. Em particular, a degradação farmacológica do IKZF1 resultou na redução do crescimento celular, enfatizando o seu importante papel na regulação positiva do CRC, que é crítico para a proliferação e sobrevivência das células ALCL. Além disso, a equipe de pesquisa também mostrou que os inibidores STAT3, como STAT3-IN-3 e Stattic, podem efetivamente reduzir a viabilidade das células ALCL, e sua combinação com degradadores IKZF1 produziu efeitos antitumorais mais significativos.
Um dos principais insights deste estudo é a interação entre STAT3 e MYC. Ao usar o ChIP-seq, os pesquisadores descobriram que o STAT3 se liga à região regulatória superpotenciadora do gene MYC, produzindo altos níveis de proteína MYC, e então coopera com os fatores de transcrição CRC para manter altos níveis de expressão de MYC. Esta interação destaca o potencial terapêutico de direcionar STAT3 em ALCL, particularmente em casos resistentes aos inibidores de ALK. O professor Look acrescentou: “Ao demonstrar que a ativação do STAT3 é necessária e suficiente para a expressão do MYC e a sobrevivência das células ALCL, fornecemos uma forte justificativa para o desenvolvimento de terapias direcionadas ao STAT3”.
Em conjunto, este estudo revela a complexa rede regulatória que mantém o ALCL e identifica o STAT3 como chave para o processo oncogênico. Os esforços combinados da equipe de pesquisa abrem caminho para novas estratégias terapêuticas visando as dependências transcricionais interconectadas no ALCL. Como disse o professor Look, “Nosso trabalho fornece informações importantes sobre a biologia molecular do ALCL e orienta pesquisas futuras em direção a tratamentos mais eficazes”.
Referência do diário
Prutsch, N., He, S., Berezovskaya, A., Durbin, AD, Dharia, NV, Maher, KA,… & Look, AT (2024). “STAT3 integra sinalização de tirosina quinase ativada com circuitos reguladores transcricionais centrais oncogênicos no linfoma anaplásico de células grandes.” Cell Reports Medicine, 5(101472). Número digital: https://doi.org/10.1016%2Fj.xcrm.2024.101472
Sobre o autor
Instituto do Câncer Dana-Farber
Professor de Pediatria
Faculdade de Medicina de Harvard
Boston, Massachusetts
A. Thomas LucasM.D., professor de pediatria na Harvard Medical School e membro do Departamento de Oncologia Pediátrica do Dana-Farber Cancer Institute. Look recebeu seu treinamento de medicina e pós-graduação em pediatria pela Universidade de Michigan e recebeu treinamento em oncologia pediátrica no St. Jude Children’s Research Hospital, onde se tornou presidente do Departamento de Oncologia Experimental e professor de pediatria na Faculdade de Medicina da Universidade do Tennessee ao longo de duas décadas. Em 1999, ele foi transferido do St. Jude Children’s Research Hospital para o Dana-Farber Cancer Institute e a Harvard Medical School para estabelecer um programa de pesquisa usando especificamente o peixe-zebra como modelo de câncer humano.
Nas últimas quatro décadas, Look publicou 390 artigos revisados por pares sobre a base molecular da transformação maligna, proliferação aberrante e apoptose de células cancerígenas, bem como a aplicação de descobertas genéticas moleculares para melhorar o tratamento de doenças malignas em crianças e adultos, particularmente leucemia aguda de células T, neuroblastoma e síndromes mielodisplásicas.
Look conduziu pesquisas genéticas com o objetivo de identificar novos alvos para o tratamento do câncer e agora é reconhecido internacionalmente como líder na área. Sua equipe descobriu o gene do receptor tirosina quinase do linfoma anaplásico (ALK) em 1994. Look continua mostrando que as células T da leucemia possuem uma rede transcricional “central” que é muito semelhante àquela que controla a pluripotência das células-tronco embrionárias, mudando drasticamente a visão da LLA-T como uma doença molecularmente homogênea para uma que abrange muitos subtipos diferentes. Recentemente, Look e colegas descobriram que mutações adquiridas em uma região potenciadora crítica a montante do oncogene TAL1 criam novos locais de ligação para o fator de transcrição MYB. A ligação MYB promove a ligação de outros membros do complexo TAL1 e ativa o super intensificador a montante do oncogene TAL1, conduzindo a expressão de alto nível e, por fim, formando T-ALL. Esta descoberta fornece uma estrutura conceitual para a compreensão dos eventos genéticos que transformam os timócitos humanos e o desenvolvimento de estratégias de tratamento personalizadas eficazes.
Além disso, seu laboratório desenvolveu os primeiros modelos transgênicos de peixe-zebra de leucemia linfoblástica aguda de células T e neuroblastoma infantil, proporcionando a oportunidade de aplicar poderosas técnicas de biologia genética e química adaptadas a modelos de peixe-zebra para identificar novos alvos moleculares e medicamentos de moléculas pequenas para o tratamento desses cânceres infantis. Seu laboratório também desenvolveu os primeiros modelos de peixe-zebra de síndrome mielodisplásica e hematopoiese clonal devido à perda de TET2, ASXL1 e DNMT3A, e ele está usando esses modelos para identificar drogas que visam seletivamente células-tronco hematopoiéticas mutantes e células progenitoras, preservando a função hematopoiética normal.