A fibrilação atrial (FA) é uma doença cardíaca misteriosa que afeta milhões de pessoas em todo o mundo e representa um quebra-cabeça complexo. Esta condição pode causar batimentos cardíacos irregulares, diminuir a função cardíaca e aumentar significativamente o risco de acidente vascular cerebral. Embora se saiba que a fibrilhação auricular tem uma forte componente genética, os mecanismos pelos quais as variantes genéticas comuns aumentam o risco de fibrilhação auricular permanecem indefinidos. Estudos recentes começaram a revelar como factores genéticos comuns influenciam a fibrilhação auricular, estabelecendo as bases para investigação inovadora para desvendar estes mistérios.
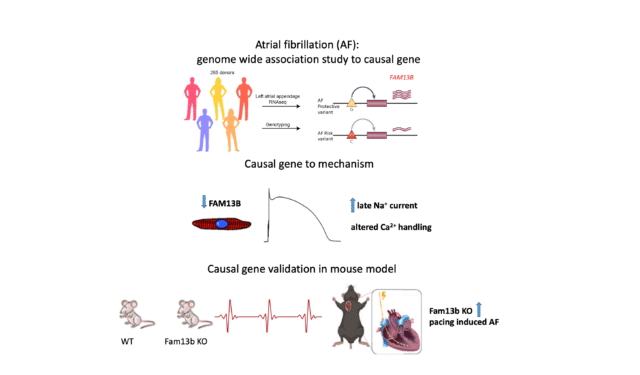
Em um estudo fundamental, os professores da Cleveland Clinic, Jonathan Smith e Mina K. Chung, Ph.D., e sua equipe colaborativa, juntamente com contribuições críticas de Gregory Tchou e Daniela Ponce-Balbuena, Ph.D., fizeram progressos significativos na compreensão da base genética da fibrilação atrial, a arritmia cardíaca mais comum. O seu estudo destaca o papel fundamental do gene FAM13B no aumento da probabilidade de desenvolver a doença, abrindo caminho para novos tratamentos personalizados.
O professor Smith compartilhou: “Embora muitas variantes genéticas raras que causam FA alterem a estrutura da proteína, as variantes mais comuns associadas ao risco de FA não alteram a estrutura da proteína, mas regulam a expressão de genes próximos, regulando assim a quantidade de proteína produzida. células que afetam sua sinalização elétrica e manipulação de cálcio, que são essenciais para batimentos cardíacos normais”. Esta visão marca um avanço significativo na compreensão desta complexa doença cardíaca.
Sua pesquisa se concentrou em como as mudanças na expressão desse gene afetam a sinalização elétrica do coração e o manejo do cálcio, que são essenciais para manter um batimento cardíaco estável. A equipe usou tecnologia avançada de edição genética, especificamente CRISPR-Cas9, para alterar especificamente esse gene em células-tronco humanas e posteriormente diferenciá-las em cardiomiócitos. Esta abordagem inovadora permite um estudo detalhado do impacto do gene na função cardíaca.
Além disso, conduziram estudos examinando a atividade elétrica das células cardíacas com atividade genética reduzida. Usando uma técnica chamada patch clamp, eles estudaram células cardíacas isoladas com atividade genética reduzida. Esses estudos são essenciais para elucidar como as alterações genéticas afetam a sinalização elétrica no coração.
Além disso, a equipe estudou como essas alterações genéticas afetam a sinalização do cálcio nas células cardíacas. Eles usaram um sistema chamado IonOptix para medir os níveis de cálcio nas células após reduzir a atividade do gene, explorando ainda mais o seu papel na função cardíaca.
Numa parte importante da sua investigação, os professores Smith e Ponce-Balbuena estudaram ratos geneticamente modificados para não possuírem o gene FAM13B. O professor Smith observou: “Esses ratos tinham certos padrões de ondas cardíacas que duravam mais e eram mais suscetíveis a problemas de ritmo cardíaco do que os ratos normais”. Esta descoberta destaca o importante papel do gene na manutenção do ritmo cardíaco normal.
Juntas, suas descobertas esclarecem o papel crítico do FAM13B na fibrilação atrial. Ao identificar genes cujos níveis de expressão alteram a função cardíaca e demonstrar o seu impacto no coração, o Professor Smith e colegas melhoraram significativamente a nossa compreensão da base genética da fibrilhação auricular. O seu trabalho abre novos caminhos para o desenvolvimento de tratamentos direcionados, potencialmente mudando a forma como esta doença cardíaca comum é tratada.
Referência do diário:
Tchou G, Ponce-Balbuena D, Liu N, Gore-Panter S, Hsu J, Liu F, Opoku E, Brubaker G, Schumacher SM, Moravec CS, Barnard J, Van Wagoner DR, Chung MK, Smith JD. A expressão reduzida de FAM13B aumenta a suscetibilidade à fibrilação atrial através da modulação das correntes de sódio e da manipulação do cálcio. Ciência Básica da Tradução JACC. 26 de julho de 2023;8(10):1357-1378. doi: https://doi.org/10.1016/j.rineng.2023.101425
Sobre o autor
Dr.é professor e presidente do Departamento de Medicina Molecular da Cleveland Clinic Lerner College of Medicine da Case Western Reserve University. Ele também é diretor do programa de treinamento de doutorado em medicina molecular. Dr. Smith faz parte da equipe do Departamento de Ciências Cardiovasculares e Metabólicas do Lerner Research Institute da Cleveland Clinic, onde ocupa a Cátedra Jeffrey Gund em Pesquisa Cardiovascular. Dr. Smith obteve bacharelado em biologia pela Universidade da Califórnia, Santa Cruz, e doutorado em biologia celular e do desenvolvimento pela Divisão de Ciências Médicas da Universidade de Harvard. Ele conduziu pesquisas de pós-doutorado no laboratório de Jan Breslow na Universidade Rockefeller, estudando a expressão do gene da apolipoproteína, o metabolismo das lipoproteínas e modelos de aterosclerose em camundongos. Smith foi promovido a professor assistente e professor associado no Rockefeller e ingressou no Instituto Lerner em 2002. Ele recebeu prêmios de carreira e reconhecimento profissional dos Institutos Nacionais de Saúde e da American Heart Association, bem como o Prêmio Excelência em Educação do Instituto Lerner. Ele publicou quase 200 artigos de pesquisa originais revisados por pares, bem como outras revisões e editoriais. A pesquisa do Dr. Smith é atualmente financiada por duas bolsas do NIH R01 e uma bolsa de projeto liderada pela Dra. Mina Chung. É também o Investigador Principal da Bolsa de Formação T32, que apoia estagiários no programa de doutoramento em Medicina Molecular. Dr. Smith treinou vários estudantes de doutorado, pós-doutorado, estudantes de medicina, técnicos de laboratório e estudantes do ensino médio e universitário. Ele apoia a entrada de estudantes de minorias sub-representadas em carreiras STEM.

Greg Zhou é tecnólogo-chefe do laboratório do Dr. Jonathan D. Smith, Departamento de Ciências Cardiovasculares e Metabólicas, Cleveland Clinic. Antes de ingressar no laboratório Smith, ele recebeu seu bacharelado e doutorado em bioquímica e biologia celular pela Universidade de Michigan. em biologia celular pela Rice University. Sua pesquisa se concentra no estudo da base genética da fibrilação atrial por meio da edição do gene CRISPR-Cas9 em modelos de células-tronco humanas. Ele gosta de jogar futebol, andar de bicicleta pelos muitos parques metropolitanos pitorescos de Cleveland quando o tempo da cidade permite e (frequentemente) jogar jogos de tabuleiro quando o tempo permite.

Dra. Daniela Ponce Balbuenaconcluiu seu bacharelado e mestrado na Universidade Autônoma de Benemerita, Puebla. Puebla, México. Ela recebeu seu doutorado pela Universidade de Colima. Em 2011, veio para Colima, no México, e depois mudou-se para os Estados Unidos para atuar como pesquisador de pós-doutorado no Centro de Pesquisa de Arritmia da Universidade de Michigan. Em 2020, ela ingressou no Departamento de Fisiologia e Biologia Celular da Universidade Estadual de Ohio e no Davis Heart and Lung Institute como professora assistente de pesquisa. Em 2023, ingressou na Divisão de Medicina Cardiovascular do Departamento de Medicina da Escola de Medicina e Saúde Pública da UW-Madison, onde atualmente atua como Cientista III. A investigação de Daniela centra-se na regulação dos canais iónicos cardíacos e nos mecanismos de arritmia. O objetivo de sua pesquisa é descobrir novos alvos de medicamentos para prevenir e/ou tratar arritmias cardíacas. Daniela aproveita a vida como cientista e atribui seu sucesso como investigadora à excelente equipe de cientistas com quem tem o privilégio de trabalhar.