UreG é um acompanhante molecular que desempenha um papel na ativação da urease, uma enzima dependente de níquel necessária para a infecção do hospedeiro por muitas bactérias e fungos patogênicos. A UreG também atua como uma GTPase, cooperando com outros parceiros para direcionar a energia da hidrólise do GTP e fornecer os íons de níquel necessários para ativar a urease, desempenhando assim um papel fundamental nos ecossistemas celulares e nas vias de homeostase dos metais.
Elisabetta Mileo do laboratório BIP (Universidade de Aix-Marseille e CNRS) e a professora Barbara Zambelli do Departamento de Farmácia e Biotecnologia (Universidade de Bolonha), juntamente com a professora Valérie Belle, o professor Bruno Guigliarelli, o Dr. comportamento da proteína GTPase UreG dentro de células bacterianas vivas. Isto representa um grande avanço na nossa compreensão da função das proteínas em habitats naturais. O seu estudo, publicado na prestigiada revista iScience, ilustra como a proteína UreG – necessária para a activação da urease em bactérias – apresenta uma flexibilidade notável na sua competição fisiológica, o que pode ser crítico para a sua actividade enzimática.
O papel do UreG como acompanhante para ajudar a ativar enzimas dependentes de níquel, como a urease, foi previamente bem documentado através de estudos in vitro que demonstraram o comportamento flexível da enzima em solução. Esses dados avançam a compreensão através da implantação de marcação de spin direcionada ao local combinada com espectroscopia de ressonância paramagnética eletrônica (SDSL-EPR) para observar diretamente o comportamento de UreG em células vivas.
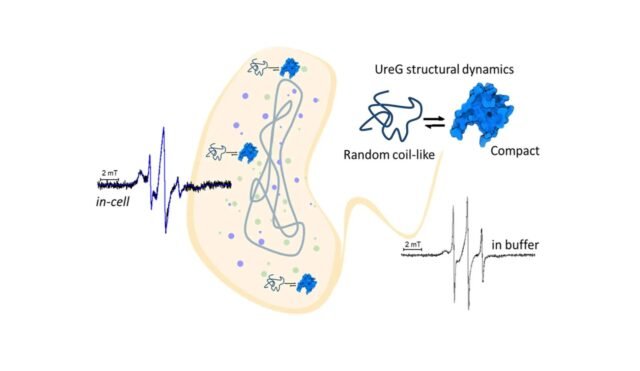
Dr Zambelli destacou a importância do estudo, dizendo: “As descobertas sugerem que a UreG mantém um cenário estrutural diversificado Integradoexistindo em dois grupos principais de conjuntos conformacionais, exibindo propriedades aleatórias semelhantes a bobinas ou compactas. Estes insights confirmam o significado fisiológico da natureza desordenada intrínseca da UreG e sugerem que o papel da flexibilidade proteica para esta enzima específica pode estar relacionado com a regulação de uma ampla gama de interações proteicas pela entrega de íons metálicos. “
Os pesquisadores usaram técnicas inovadoras para aprofundar o comportamento da proteína UreG em um ambiente celular. “Integrado “Os experimentos EPR começam marcando a proteína alvo produzida pela expressão recombinante e depois entregando-a na célula”, explicou o Dr. Mileo. Este estudo utilizou um protocolo de entrega envolvendo íons de cálcio e um breve choque térmico (incubação a 42°C) para promover a internalização ideal da proteína, mantendo assim a viabilidade celular.
Este estudo não apenas destaca a desordem inerente e a flexibilidade da proteína UreG, mas também marca um grande avanço metodológico no estudo de proteínas em seu ambiente celular nativo. “A aplicação de spin tags à base de nitróxido permite que a análise EPR seja realizada à temperatura ambiente, sob condições consistentes com o tempo de vida das células em estudo”, acrescentou o Dr. Mileo, destacando a capacidade do método de observar proteínas em seu ambiente natural sem comprometer a saúde celular. Ao utilizar espectroscopia SDSL-EPR avançada, a equipe de pesquisa forneceu informações valiosas sobre a paisagem conformacional do UreG, estabelecendo as bases para esforços futuros destinados a revelar os mecanismos complexos da função proteica em células vivas. Esta investigação não só aprofunda a nossa compreensão da dinâmica das proteínas, mas também abre novos caminhos para o desenvolvimento de terapias direcionadas e aplicações biotecnológicas para a descoberta de novos medicamentos e moléculas antimicrobianas.
Referência do diário
Annalisa Pierro et al., “Estudo intracelular da paisagem conformacional da GTPase UreG por SDSL-EPR,” iScience, 2023.
Número digital: https://doi.org/10.1016/j.isci.2023.107855.
Sobre o autor
Bárbara Zambelli – Professora Associada desde 2021 e Professora Auxiliar da UniBO desde 2008. Suas atividades de pesquisa visam a compreensão em nível molecular e estrutural, Interações de proteínas baseadas em metais Nos sistemas biológicos, é responsável pela regulação de processos metabólicos importantes para a vida. Em particular, os seus principais interesses de investigação envolvem o metabolismo celular níquel e seu impacto saúde humanacom possíveis aplicações médicas e farmacêuticas.

Elizabeth Mileo é pesquisador do CNRS no laboratório “Bioénergétique et Ingénierie des Protéines” (BIP) em Marselha, França. Ela é química e espectroscopista com vasta experiência na síntese e uso de radicais nitróxidos como marcadores de spin em biologia estrutural. As atividades de investigação da E. Mileo centram-se no estudo da dinâmica estrutural das proteínas, em particular chaperonas moleculares e outras proteínas flexíveis, com o objetivo de obter informação sobre como a dinâmica das proteínas influencia a função das proteínas. A originalidade do seu trabalho reside no fato de que o SDSL-EPR estuda proteínas diretamente dentro das células (Integrado EPR), sob condições fisiológicas. Sua pesquisa também visa desenvolver novas ferramentas e novos spin tags para rastrear proteínas que “fazem seu trabalho” diretamente nas células vivas via EPR.