Os lipídios constroem membranas celulares e organelas, algumas das quais atuam como moléculas sinalizadoras essenciais na regulação da função celular. Os lipídios também são fonte de energia, mas seu acúmulo excessivo no organismo pode levar à obesidade. A obesidade é um problema significativo em todo o mundo e o uso de métodos tradicionais, como exercícios e dieta alimentar, para prevenir a obesidade pode nem sempre ser eficaz. Felizmente, a ciência pode fornecer soluções úteis com base nas especificidades do metabolismo da gordura. O metabolismo lipídico envolve a síntese e quebra de lipídios, auxiliada por uma variedade de enzimas que regulam todo o processo. Ao compreender como estas enzimas funcionam, novos tratamentos para a obesidade e outras doenças associadas a defeitos no metabolismo lipídico poderão ser desenvolvidos.
A pesquisa pioneira realizada por uma equipe liderada pela professora Katarzyna Kwiatkowska, do Instituto Nencki de Biologia Experimental, em Varsóvia, revelou um mecanismo até então desconhecido que regula o desempenho das enzimas do metabolismo lipídico. A equipe era composta por Gabriela Traczyk, Aneta Hromada-Judycka, Anna Świątkowska, Anna Ciesielska e Julia Wiśniewska, que desempenharam um papel importante na descoberta. Suas descobertas, publicadas no Journal of Lipid Research, representam um grande avanço na compreensão da sinalização celular e do metabolismo lipídico.
Os cientistas usaram técnicas sofisticadas para identificar modificações específicas da molécula de diacilglicerol quinase-ε (DGKε), S-Palmitoilação, que envolve a adição de resíduos de ácidos graxos (ácido palmítico, um componente comum da gordura alimentar) à enzima. Esses métodos rigorosos incluem a clonagem de variantes de DGKε com resíduos de aminoácidos únicos alterados em relação à forma nativa, a transfecção de DGKε em células renais humanas cultivadas e a utilização de técnicas químicas especializadas (por exemplo, química baseada em cliques). Essas técnicas destacam a precisão e o rigor da pesquisa, resultando em resultados confiáveis.
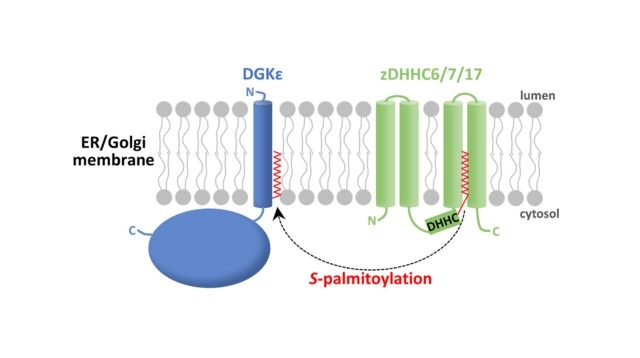
O professor Kwiatkowska explica: “No nosso estudo identificamos primeiro uma cisteína específica, S-Palmitoilação em DGKε. Este aminoácido está localizado no lado citoplasmático do DGKε integrado nas membranas das organelas. Em seguida, usamos duas técnicas de marcação complementares (acil polietilenoglicol e troca de acil biotina) para revelar a enzima (denominada zDHHC) que realiza: S-Palmitoilação. Encontramos evidências conclusivas de DGKε S-A palmitoilação pode afetar a conversão do diacilglicerol em ácido fosfatídico, uma etapa crítica na síntese de certos lipídios.
Os cientistas também usaram micelas contendo diacilglicerol para examinar a atividade das enzimas estudadas e descobriram que a atividade do DGKε S-Palmitoilação. Micelas são pequenas estruturas esféricas formadas a partir de moléculas, como o diacilglicerol, com regiões hidrofóbicas e hidrofílicas em soluções aquosas. Os pesquisadores também examinaram a localização celular do DGKε e, além de detectar o DGKε no retículo endoplasmático onde a maioria dos lipídios é sintetizada, também encontraram a quinase no aparelho de Golgi. Eles especulam sobre a probabilidade de impacto S-Efeitos da palmitoilação de DGKε no seu tráfego e localização celular.
Traczyk, MSc, explica: “Nossos resultados indicam que uma pequena porção de DGKε está presente no Golgi, levando-nos a propor que ele está envolvido em aspectos específicos da síntese lipídica. Embora estudos adicionais de DGKε nativo possam revelar o papel exato de DGKε no Golgi, nosso estudo abre novos caminhos para estudar o envolvimento desta enzima no ciclo de sinalização de fosfoinositídeo e no metabolismo lipídico em geral. ”
Este estudo inovador da equipe do Professor Kwiatkowska mostra: S-A palmitoilação pode ajustar a atividade DGKε em compartimentos celulares específicos. Isto irá melhorar significativamente a nossa compreensão da sinalização celular e do metabolismo lipídico e abrir caminho para novas estratégias de tratamento para a obesidade e outras doenças.
Referência do diário
Gabriela Traczyk, Aneta Hromada-Judycka, Anna Świątkowska, Julia Wiśniewska, Anna Ciesielska, Katarzyna Kwiatkowska). “A diacilglicerol quinase-ε é S-palmitoilada na cisteína no terminal citoplasmático de seu segmento transmembranar N-terminal.” Journal of Lipid Research, 65 (1) (2023) 100480. doi: https://doi.org/10.1016/j.jlr.2023.100480
Sobre o autor
Gabriella Traczyk é estudante de doutorado e trabalha no Laboratório de Biologia Molecular de Membranas, Instituto Nencki de Biologia Experimental, Varsóvia. Sua pesquisa se concentra na função da DGKε quinase. Mutações no gene que codifica DGKε causam uma doença renal chamada síndrome hemolítico-urêmica atípica (SHUa), e a pesquisa da Sra. Traczyk visa elucidar o impacto dessas mutações na estabilidade do DGKε e na atividade enzimática. Ela também é a principal coautora do estudo, que revelou S-Palmitoilação de DGKε (ORCID: https://orcid.org/0000-0003-2065-440X).

Aneta Hromard Judicaé pesquisador de pós-doutorado no Laboratório de Biologia de Membranas Moleculares, Instituto Nencki de Biologia Experimental, Varsóvia. Ela recebeu seu doutorado em 2011 e ingressou no laboratório em 2013. Sua pesquisa se concentra na elucidação dos mecanismos moleculares da sinalização do TLR4. O TLR4 é um receptor de membrana plasmática ativado por lipopolissacarídeo bacteriano (LPS) durante a infecção, e a atividade descontrolada do TLR4 pode levar à sepse. Dr. Hromada-Judycka estudou o papel dos lipídios, especificamente derivados do fosfatidilinositol, na cascata de sinalização do receptor TLR4. Ela é coautora de um estudo proteômico sobre palmitoilação de proteínas em macrófagos estimulados por LPS, que revelou que a DGKε quinase, uma das enzimas que controlam os níveis de fosfatidilinositol, é modificada por: S-Palmitoilação. O trabalho aqui apresentado (do qual o Dr. Hromada-Judycka é o principal coautor) é resultado desta descoberta (ORCID: https://orcid.org/0000-0002-4449-882X).