Os cientistas descobriram um mecanismo genético que pode fornecer novas formas de tratar uma infecção fúngica rara, mas mortal, que forçou o encerramento de unidades de cuidados intensivos em vários hospitais. A descoberta oferece uma esperança inicial na luta contra um patógeno que é difícil de controlar e quase impossível de tratar depois de se espalhar.
Candida auris É especialmente perigoso para pessoas que já estão gravemente doentes, deixando os hospitais altamente vulneráveis a surtos. Embora o fungo possa viver na pele sem causar sintomas, os pacientes dependentes de ventilação correm maior risco. Quando ocorre uma infecção, cerca de 45% dos pacientes morrem e o fungo é resistente a todos os principais tipos de medicamentos antifúngicos. Esta resistência torna o tratamento extremamente desafiador e permite que o patógeno persista nas enfermarias do hospital.
Ameaça global à saúde com origens misteriosas
A infecção foi descoberta pela primeira vez em 2008 e suas origens permanecem obscuras. Desde então, mais de 40 países, incluindo o Reino Unido, relataram surtos. Candida auristambém conhecido como Candida aurisé agora considerado uma grave ameaça à saúde global e aparece na lista de patógenos fúngicos prioritários da Organização Mundial da Saúde. No Reino Unido, os casos notificados continuam a aumentar de forma constante.
Estudando infecção em modelos in vivo
Pesquisadores da Universidade de Exeter deram agora um grande passo em frente, estudando como os genes Candida auris Infectar. Isto marca a primeira vez que tal atividade genética foi estudada num hospedeiro vivo usando uma abordagem baseada em larvas de peixes. A pesquisa foi publicada na revista Nature Communications Biology e foi apoiada pela Wellcome, pelo Medical Research Council (MRC) e pelo National Center for Replacement, Reduction and Refinement (NC3Rs).
Se o mesmo comportamento genético for confirmado durante a infecção humana, os resultados poderão ajudar a identificar alvos biológicos para novos tratamentos antifúngicos ou mesmo a reutilizar medicamentos existentes, dizem os investigadores.
O projeto é co-liderado por Hugh Gifford, professor clínico do NIHR no MRC Center for Medical Mycology (CMM) da Universidade de Exeter. Ele disse: “Desde o seu surgimento, Candida auris Causou estragos nas unidades de terapia intensiva dos hospitais. Para os pacientes vulneráveis, pode ser fatal e os fundos de saúde gastaram milhões no assustador esforço de erradicação. Acreditamos que o nosso estudo pode revelar um calcanhar de Aquiles deste agente patogénico mortal durante a infecção activa, e precisamos urgentemente de mais investigação para explorar se podem ser encontrados medicamentos que visem e explorem esta vulnerabilidade. “
Por que os modelos de pesquisa tradicionais são insuficientes
Um dos maiores obstáculos na aprendizagem Candida auris tem sido sua capacidade de sobreviver a altas temperaturas. Juntamente com a sua tolerância invulgarmente forte ao sal, alguns investigadores acreditam que pode ter origem em oceanos tropicais ou em animais marinhos. Essas características também dificultam a realização de pesquisas utilizando modelos laboratoriais tradicionais.
Para superar este problema, a equipe de Exeter desenvolveu um novo modelo de infecção utilizando o killifish árabe. Os ovos desta espécie podem sobreviver a temperaturas semelhantes às do corpo humano, tornando-os adequados para observar infecções em condições muito semelhantes às de doenças reais.
Atividade genética revela possível vulnerabilidade
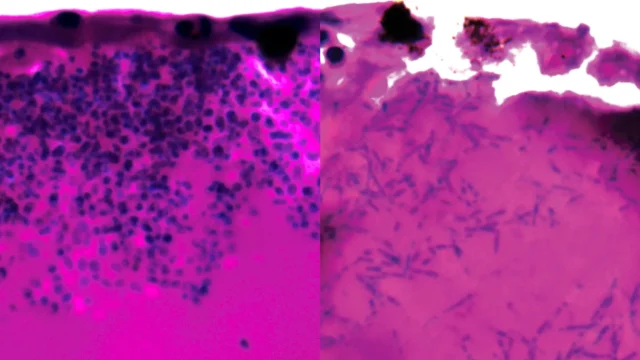
Durante o experimento, os pesquisadores observaram Candida auris Sua forma pode ser alterada formando estruturas fúngicas alongadas chamadas filamentos. Essas estruturas podem ajudar o fungo a encontrar nutrientes ao infectar seu hospedeiro.
A equipe também analisou quais genes são ativados ou desligados durante a infecção para identificar possíveis vulnerabilidades. Alguns dos genes que se tornaram ativos foram responsáveis pela produção de bombas de nutrientes que capturam moléculas eliminadoras de ferro e entregam o ferro às células fúngicas. Dado que o ferro é essencial para a sobrevivência, este processo pode representar uma vulnerabilidade grave.
O coautor sênior, Rhys Farrer, do Centro MRC de Micologia Médica da Universidade de Exeter, disse:”Até agora não sabíamos quais genes estão ativos durante a infecção em um hospedeiro vivo. Agora precisamos descobrir se isso também ocorre durante a infecção em humanos. O fato de descobrirmos que os genes são ativados para eliminar o ferro nos dá uma pista. Candida auris Pode originar-se de ambientes com deficiência de ferro no oceano. Também nos fornece alvos potenciais para medicamentos novos e existentes. “
Esperança para tratamentos futuros
Dr. Gifford, que também é médico residente em cuidados intensivos e medicina respiratória no Royal Devon and Exeter Hospital, enfatizou a importância clínica das descobertas. Ele disse: “Embora ainda haja muitas etapas de pesquisa a serem concluídas, nossas descobertas podem levar a perspectivas animadoras para tratamentos futuros. Temos medicamentos que têm como alvo a atividade de eliminação de ferro. Agora precisamos explorar se eles podem ser reaproveitados para bloquear a atividade de eliminação de ferro”. Candida auris Desde matar humanos e fechar unidades de terapia intensiva de hospitais. “
O modelo larval de killifish árabe foi desenvolvido com o apoio de uma bolsa de projeto NC3Rs como uma alternativa aos modelos de camundongos e peixes-zebra que são comumente usados para estudar interações entre patógenos e seus hospedeiros. A Dra. Katie Bates, Diretora de Bolsas de Pesquisa da NC3Rs, disse: “Esta nova publicação demonstra a utilidade de modelos alternativos na pesquisa Candida auris infecção e permitir insights sem precedentes sobre os eventos celulares e moleculares do hospedeiro vivo infectado. Este é um excelente exemplo de como alternativas inovadoras podem superar as principais limitações da investigação animal tradicional. “
O artigo é intitulado “Expressão do gene do transportador de xenosideróforos e filamentação específica do clado”. Candida auris peixe matador (Afânio é diferente) infecção” e publicado na revista Nature biologia da comunicação.