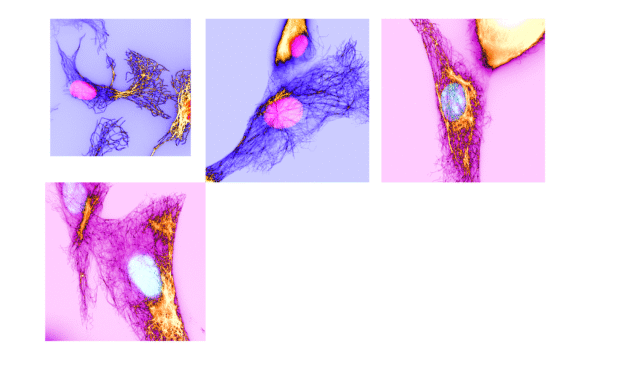
Os microtúbulos são essenciais para a divisão celular e integridade estrutural e desempenham um papel importante na dinâmica das células cancerígenas. Drogas como o paclitaxel usadas na quimioterapia têm como alvo essas estruturas, estabilizando-as para inibir a divisão celular. No entanto, a descoberta da UNC-45A, uma proteína de corte de microtúbulos independente de ATP, lançou uma nova luz sobre esta dinâmica.
A professora Martina Bazzaro e sua equipe da Universidade de Minnesota (incluindo Asumi Hoshino, Dr. Valentino Clemente, Mihir Shetty, Dr. Brian Castle e Professor David Odde) descobriram o papel único do UNC-45A na dinâmica dos microtúbulos, abrindo novos caminhos para a pesquisa do tratamento do câncer.
Para explorar o papel do UNC-45A, a equipe usou uma combinação de reconstruções biofísicas in vitro e análise de microscopia de fluorescência interna total. Eles recriaram condições celulares em um ambiente controlado para observar como o UNC-45A interage com os microtúbulos, concentrando-se em sua preferência de ligação por microtúbulos curvos em vez de retos. Além disso, eles manipularam os níveis de UNC-45A nas células para observar seu efeito na curvatura dos microtúbulos.
O professor Bazzaro explica: “A ruptura do MT mediada por UNC-45A precede o início da flexão do MT. Embora os MTs sejam biopolímeros rígidos nas células, eles frequentemente se dobram, e o resultado dessa flexão pode ser a quebra.” Esta percepção destaca o mecanismo único pelo qual o UNC-45A afeta o comportamento dos microtúbulos, que é diferente das habituais proteínas de ruptura dependentes de ATP.
Uma descoberta surpreendente do estudo mostrou que o UNC-45A causou curvatura dos microtúbulos mesmo na presença de paclitaxel. Embora se saiba que o paclitaxel endireita os microtúbulos, a equipa observou que os microtúbulos tratados com paclitaxel tornaram-se menos rígidos e mais ondulados in vitro, mas endireitaram-se num ambiente celular.
Esta descoberta tem implicações profundas para a compreensão da resistência das células cancerígenas à quimioterapia. O professor Bazzaro observou: “Apesar deste[efeito de alisamento do paclitaxel]o UNC-45A mantém a sua capacidade de induzir flexão em MTs expostos ao paclitaxel”. Isto sugere que o UNC-45A pode desempenhar um papel no desenvolvimento da resistência à quimioterapia em células cancerígenas, apresentando novos desafios e oportunidades para intervenção terapêutica.
Esta investigação é crítica não só em oncologia, mas também para a compreensão de outras doenças que envolvem a perturbação da dinâmica dos microtúbulos, como as doenças neurodegenerativas. O mecanismo único independente de ATP do UNC-45A pode ter vantagens em doenças caracterizadas por níveis reduzidos de ATP e alto estresse oxidativo.
Tomados em conjunto, o estudo da Universidade de Minnesota fornece informações importantes sobre o papel do UNC-45A na dinâmica dos microtúbulos e abre novas possibilidades para o tratamento de doenças onde a estabilidade dos microtúbulos é crítica. Estas descobertas abrem caminho para tratamentos mais eficazes e direcionados, enriquecendo a nossa compreensão das estruturas celulares e das suas interações com os medicamentos.
Referência do diário
Martina Bazzaro, Asumi Hoshino, Valentino Clemente, Mihir Shetty, Brian Castle, David Odde, “A proteína de corte de microtúbulos UNC-45A liga-se preferencialmente a microtúbulos dobrados e neutraliza os efeitos de endireitamento de microtúbulos do paclitaxel”, Journal of Biological Chemistry, 2023. https://doi.org/10.1016/j.jbc.2023.105355
Sobre o autor
Dr. Bazaro é professora associada titular do Departamento de Obstetrícia, Ginecologia e Saúde da Mulher e do Masonic Cancer Center da Universidade de Minnesota. Ela recebeu seu doutorado. Doutor em Química Medicinal pelo Departamento de Ciências Farmacêuticas da Universidade de Ferrara, Itália. Dr. Bazzaro atuou como pesquisador visitante no “Instituto de Bioquímica” em Lausanne, Suíça, e no Instituto Karolinska em Estocolmo, Suécia. Ela completou seu treinamento de pós-doutorado no Departamento de Patologia do Hospital Johns Hopkins.
Dr. Bazzaro tem um interesse de pesquisa ao longo da vida em câncer cervical e de ovário. Ela combina experiência em biologia do câncer de ovário e química medicinal para descobrir medicamentos personalizados para mulheres com câncer cervical e de ovário para as quais a quimioterapia tradicional não é uma opção satisfatória. O laboratório do Dr. Bazzaro estuda anormalidades nas vias de degradação de proteínas no câncer de mama e de ovário. O sistema ubiquitina-proteassoma (UPS) é responsável pela degradação de mais de 90% das proteínas intracelulares de vida curta. A degradação de proteínas pelo sistema ubiquitina-proteassoma é um processo de múltiplas etapas que começa com a desubiquitinação de moléculas alvo marcadas com ubiquitina por enzimas desubiquitinantes, seguida pela sua entrada no compartimento catalítico 20S do proteassoma (onde realmente ocorre a degradação). Os alvos peptídicos do proteassoma incluem proteínas envolvidas na progressão, sobrevivência e inflamação do ciclo celular. Embora a degradação proteasomal dependente da ubiquitina seja crítica para células normais e malignas, a maior demanda por atividade metabólica/catabólica associada a fenótipos malignos torna a via ubiquitina-proteassoma uma ferramenta adequada para a terapia do câncer. O laboratório está particularmente interessado em estudar o papel das vias de degradação de proteínas assistidas por proteassoma e lisossoma no desenvolvimento e progressão do cancro da mama e do ovário e no desenvolvimento de novos inibidores de moléculas pequenas do sistema ubiquitina-proteassoma contra células cancerígenas da mama e do ovário.