O adenocarcinoma ductal pancreático (PDAC) é um rival formidável no mundo do câncer, conhecido por sua progressão insidiosa e impacto devastador. É uma das principais causas de morte relacionada ao câncer em todo o mundo e espera-se que cresça como uma das principais causas na próxima década. A letalidade do PDAC reside na sua natureza agressiva, localização anatômica profunda do pâncreas, diagnóstico tardio frequente e notória reputação de não aceitar tratamentos convencionais limitados. Esta situação crítica destaca a necessidade urgente de a comunidade científica tomar medidas para decifrar os mistérios moleculares que impulsionam o progresso contínuo do PDAC e preparar o caminho para intervenções terapêuticas inovadoras e eficazes.
O PDAC, conhecido pelo seu ambiente de tratamento agressivo e desafiador, poderá em breve enfrentar novos concorrentes na luta contra a progressão do câncer. O professor Upender Manne, da Universidade do Alabama em Birmingham, e colegas colaboraram com pesquisadores da Universidade de Washington em St. Louis e da Universidade do Texas Rio Grande Valley para publicar um estudo inovador em uma revista revisada por pares. neoplasia. Os resultados lançam luz sobre um novo alvo terapêutico: TRIP13. Esta proteína é superexpressa em tumores PDAC e desempenha um papel importante no crescimento tumoral, metástase e resistência à quimioterapia.
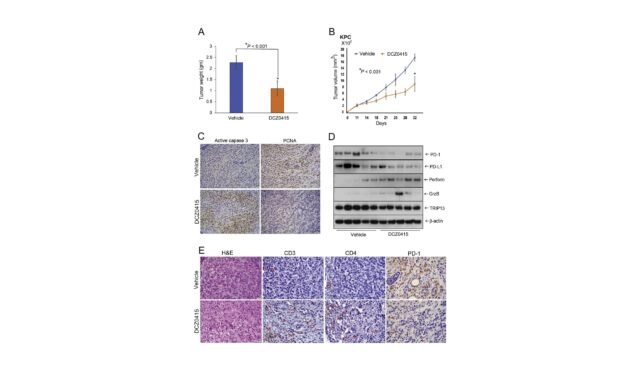
A abordagem inovadora deste estudo centra-se no nocaute genético do TRIP13 e na sua inibição farmacológica utilizando o inibidor de moléculas pequenas DCZ0415. O professor Manne e seus colegas documentaram meticulosamente o impacto significativo da inibição do TRIP13 na proliferação, invasão, migração e metástase de células PDAC. A interrupção das principais vias de sinalização associadas à progressão do câncer marca um importante passo em frente nas estratégias de tratamento do PDAC.
A base desta excelente pesquisa é uma estrutura metodológica diversificada e robusta. Inicialmente, a equipe de pesquisa procurou compreender o papel oncogênico do TRIP13 no PDAC. Eles descobriram que o TRIP13 atua como um promotor do crescimento e metástase do PDAC. Notavelmente, direcionar o TRIP13 com o inibidor DCZ0415, sozinho ou em combinação com tratamentos padrão, pode prevenir eficazmente a progressão do PDAC caracterizado pela alta expressão do TRIP13.
Para explorar este papel no espectro do comportamento das células PDAC, a equipe utilizou múltiplas linhas celulares humanas de PDAC, demonstrando uma variedade de origens genéticas. “Adquirimos linhas celulares humanas PDAC exibindo vários estados mutacionais. Estas linhas celulares desempenharam um papel importante na nossa análise abrangente”, explica o professor Manne.
Um aspecto fundamental do estudo foi a avaliação do potencial migratório das células PDAC através de um ensaio de cicatrização de feridas. Este método não só elucida o impacto da inibição do TRIP13 na migração celular, mas também fornece uma medida tangível da eficácia do inibidor. “Para os estudos de shRNA, as células silenciadas e de controle com TRIP13, bem como as células tratadas com DCZ0415, foram submetidas a ensaios de cicatrização de feridas para determinar o efeito na migração. Essa abordagem nos permitiu avaliar visual e quantitativamente o impacto do direcionamento do TRIP13 na dinâmica das células PDAC, “O professor Manne elaborou as nuances do método.
Estas descobertas são de longo alcance, fornecem uma base teórica para a realização de ensaios clínicos orientados por biomarcadores e trazem esperança para melhores estratégias de tratamento para PDAC. Ao visar o TRIP13, a investigação não só abre caminho para tratamentos potencialmente mais eficazes, mas também dá um contributo significativo para a nossa compreensão da base molecular desta doença mortal. Em resumo, a investigação inovadora do Professor Manne e da sua equipa marca um progresso significativo na luta contra o PDAC. Através de uma abordagem meticulosa e foco no papel do TRIP13 na progressão do PDAC, este estudo abre novos caminhos para intervenção terapêutica e traz esperança aos pacientes que enfrentam este diagnóstico desafiador.
Referência do diário
Farrukh Afaq, Sumit Agarwal, Prachi Bajpai, et al., “Direcionar a AAA-ATPase TRIP13 oncogênica reduz a progressão do adenocarcinoma ductal pancreático”, Neoplasia, 2024.
Número digital: https://doi.org/10.1016/j.neo.2023.100951.
Sobre o autor
Upender Manne, MA, Ph.D. Dr. Manne é professor de patologia, cirurgia e epidemiologia na Universidade do Alabama em Birmingham (UAB). Ele também é diretor da Divisão de Patologia Anatômica Translacional da Escola de Medicina da UAB, codiretor do Tissue Biobank, cientista sênior do O’Neill Comprehensive Cancer Center, cientista sênior do Centro de Pesquisa em Nutrição e Obesidade e cientista sênior do Centro de Saúde Minoritária e Pesquisa de Equidade em Saúde da Escola de Medicina Heersink. Por aproximadamente trinta anos, o professor Manne atuou como investigador principal em projetos financiados pelas séries R, P e U do NIH/National Cancer Institute (NCI). Ele publicou extensivamente nas áreas de descoberta e validação de biomarcadores moleculares de câncer e disparidades na saúde do câncer em múltiplas malignidades humanas. Ele desenvolveu vários modelos pré-clínicos de câncer (xenoenxertos e organoides derivados de pacientes) para testes experimentais de drogas. Outros aspectos da carreira académica do Professor Mann têm sido a formação de estudantes, médicos e cientistas para prosseguirem carreiras académicas produtivas na investigação do cancro.