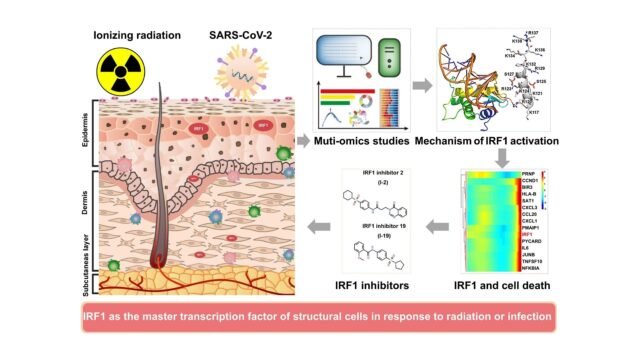
Como as células estruturais respondem ao estresse prejudicial causado pela radiação, fornecendo um meio potencial de reduzir a inflamação prejudicial e a morte celular? Os cientistas descobriram que a proteína IRF1 (fator regulador do interferon 1) torna-se ativa após a exposição à radiação, desencadeando uma reação em cadeia que pode exacerbar os danos celulares. O IRF1 é conhecido por seu papel na imunidade inata, muitas vezes ajudando o corpo a combater patógenos e células cancerígenas. A equipe liderada pelo professor Zhang Shuyu, incluindo pesquisadores da Universidade de Sichuan e da Universidade de Suzhou, como Geng Fenghao, Chen Jianhui e Song Bin, publicou os resultados da pesquisa em Imunologia Celular e Molecular.
A exposição à radiação pode causar danos graves às células, causando inflamação imediata e a longo prazo. Em importantes órgãos de barreira, como a pele, os pulmões e os intestinos, as células estruturais respondem a esse estresse, às vezes causando danos aos tecidos que se prolongam ao longo do tempo. Este estudo destaca como o IRF1, uma proteína comumente associada às respostas imunológicas, torna-se um ator central nessas respostas quando as células estruturais são expostas à radiação. Os pesquisadores descrevem detalhadamente como a radiação ativa o IRF1 e, com o apoio de proteínas acessórias específicas e modificações químicas, ajusta a atividade do IRF1 depois que ele é produzido dentro da célula.
Os experimentos cuidadosos da equipe revelaram como a radiação afeta a ativação e expressão do IRF1. Usando técnicas precisas para estudar o RNA em células individuais, eles descobriram que a exposição à radiação leva ao aumento da ativação do IRF1 em certas células da pele, como fibroblastos e queratinócitos. Surpreendentemente, esta resposta foi restrita às células estruturais e não às células imunes, sugerindo que o IRF1 tem um papel além das funções imunológicas tradicionais e pode afetar tipos de células não imunes de maneiras significativas.
De forma emocionante, os pesquisadores descobriram novas modificações no IRF1 que controlam a atividade da proteína após sua formação. Especificamente, eles descobriram que a acetilação e a fosforilação da sequência de localização nuclear do IRF1 permitem que ele se mova para o núcleo e desencadeie uma resposta inflamatória. A alteração desses locais de sequência de localização nuclear impede que o IRF1 se mova para o núcleo, onde normalmente inicia uma cascata de reações que levam à inflamação e à morte celular. O professor Zhang explicou: “Com estas descobertas, demonstramos que o movimento nuclear do IRF1 é crítico para desencadear respostas inflamatórias induzidas pela radiação”. Esta descoberta sugere que o direcionamento desses pontos de modificação poderia fornecer uma nova maneira de controlar os danos inflamatórios associados à exposição à radiação.
A tentativa e erro se concentrou em como diferentes doses e horários de radiação afetaram o comportamento do IRF1 ao longo do tempo. Quando as células foram repetidamente expostas a doses baixas, imitando um regime típico de tratamento de radiação, os níveis de ativação do IRF1 aumentaram constantemente – um efeito não observado com uma única exposição a altas doses. Esta resposta relacionada à dose significa que o papel do IRF1 na inflamação pode variar dependendo do tipo e frequência da radiação, um insight que pode ajudar a informar o projeto da radioterapia e formas de reduzir seus efeitos colaterais.
Além disso, as respostas inflamatórias induzidas pela radiação são particularmente relevantes para pacientes com cancro. A radiação ionizante, amplamente utilizada no tratamento do câncer, costuma causar lesões cutâneas dolorosas em quase todos os pacientes submetidos à radioterapia. Esta inflamação das células da pele pode afetar seriamente a qualidade de vida. Dado que a maioria dos pacientes com cancro são susceptíveis a danos na pele induzidos pela radiação, esta investigação pode abrir caminho para opções de tratamento eficazes que possam proporcionar o alívio tão necessário.
Inesperadamente, o estudo também revelou o papel de equilíbrio de uma proteína acessória chamada proteína 1 de ligação ao DNA de fita simples (SSBP1), que limita o movimento do IRF1 para o núcleo e inibe sua ativação. Quando os níveis de SSBP1 diminuem, é mais provável que o IRF1 atinja o núcleo, causando inflamação mais grave e morte celular. Esta descoberta destaca como proteínas essenciais como a SSBP1 ajudam a controlar as respostas ao estresse nas células, retardando a ativação do IRF1 e protegendo potencialmente as células da inflamação excessiva.
Além dessas descobertas, os pesquisadores estão explorando tratamentos potenciais, identificando dois inibidores de pequenas moléculas que limitam especificamente a ativação do IRF1. Os primeiros testes destes compostos mostram-se promissores na redução da inflamação e dos danos causados pela radiação, tornando-os candidatos promissores para aplicação clínica para mitigar os efeitos secundários induzidos pela radiação. Com mais testes, estes inibidores poderão ser adicionados à gama de tratamentos disponíveis para controlar os danos causados pela radiação em pacientes, especialmente aqueles submetidos a tratamento contra o cancro.
Curiosamente, esta pesquisa também se cruza com pesquisas sobre infecções virais. Foi demonstrado que o SARS-CoV-2, o vírus que causa o COVID-19, desencadeia uma inflamação semelhante nas células causada pelo IRF1. As descobertas da equipe sugerem que as proteínas virais do SARS-CoV-2 podem ativar a radiação semelhante à IRF1, levando a um processo inflamatório semelhante. A sua análise descobriu que a proteína viral NSP-10 desempenha especificamente um papel na ativação do IRF1, o que pode contribuir para os danos nos tecidos observados em casos graves de COVID-19. De forma encorajadora, os inibidores de moléculas pequenas identificados neste estudo também demonstraram inibir a ativação do IRF1 associada ao SARS-CoV-2, sugerindo o seu potencial mais amplo no tratamento da inflamação de múltiplas causas.
Novos tratamentos poderão um dia concentrar-se em medicamentos que bloqueiem ou limitem a ativação do IRF1, proporcionando uma forma promissora de proteger os pacientes dos efeitos inflamatórios a longo prazo da radioterapia. Ao concentrar-se no controle das modificações químicas do IRF1 e das ações das proteínas auxiliares, os cientistas esperam prevenir alguns dos danos celulares associados à exposição repetida à radiação, como observado em tratamentos médicos.
Esta investigação fornece novos conhecimentos sobre como as células estruturais contribuem para a inflamação sob stress, abrindo caminho para tratamentos anti-inflamatórios que poderiam ajudar não só as pessoas afetadas pela radiação, mas também indivíduos com doenças como a COVID-19, onde podem ocorrer respostas inflamatórias semelhantes. Liderada pelo professor Zhang Shuyu, um conhecido cientista na área de pesquisa de radiação nuclear, a equipe fez progressos significativos na elucidação do papel do IRF1 na proteção celular e no controle de danos. O trabalho do professor Zhang em radiobiologia e inflamação resultou em mais de 150 publicações e avançou significativamente na compreensão das lesões radiogênicas e nas opções de tratamento para pacientes que enfrentam efeitos colaterais da radiação.
Referência do diário
Geng F, Chen J, Song B, et al., “A ativação de IRF1 mediada por Chaperone e PTM inibe a morte celular induzida por radiação e respostas inflamatórias.” Imunologia Celular e Molecular, 2024. doi: https://doi.org/10.1038/s41423-024-01185-3