Abaixo da superfície do minúsculo verme transparente Caenorhabditis elegans, os pesquisadores descobriram novas pistas sobre como certas estruturas semelhantes a cabelos nas células, chamadas cílios, crescem de maneira sincronizada. Os cílios são pequenas projeções que ajudam as células a sentir o ambiente e a movimentar materiais. Essas estruturas ajudam o verme a detectar seu ambiente e geralmente crescem lado a lado em pares. Como esses pares permanecem consistentes à medida que crescem tem sido um mistério até agora. Os cientistas compreendem agora que uma proteína chamada ARL13B, envolvida na organização e sinalização destas estruturas, desempenha um papel fundamental na gestão deste crescimento lado a lado, um padrão que descrevem como “alongamento cílios-cílios justapostos”, o que significa que dois cílios adjacentes crescem em sincronia um com o outro.
Os pesquisadores da Universidade Abdullah Gul, Merve Gul Turan, Hanife Kantarci, Sebiha Cevik, Ph.D., e Oktay Kaplan, Ph.D., exploraram esse fenômeno e como o ARL13B e outras moléculas apoiam o crescimento coordenado dos cílios. Suas descobertas foram publicadas na revista iScience.
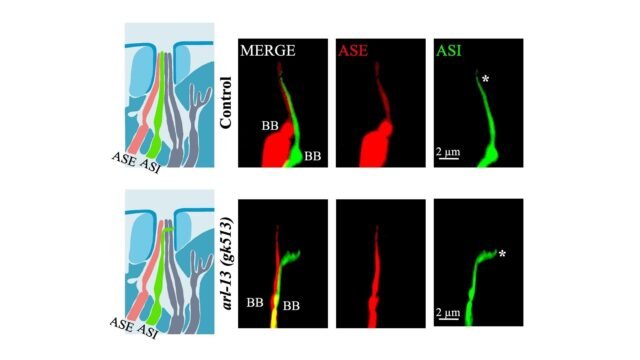
Olhando atentamente sob um microscópio usando marcadores luminescentes especiais – uma ferramenta que usa fluorescência para destacar partes específicas das células – os cientistas rastrearam como algumas das células nervosas sensoriais do verme desenvolvem cílios aos pares. Na cabeça do verme, essas saliências se estendem lado a lado e na cauda formam uma estrutura em forma de Y. Embora o comprimento real de cada cílio possa variar, o padrão de crescimento pareado permanece o mesmo. No entanto, quando falta a proteína ARL13B, os cílios já não se encontram adequadamente e, em muitos casos, apontam em direções diferentes.
Estranhamente, esse desalinhamento ocorreu apesar do comprimento dos cílios ser aproximadamente o mesmo dos nematóides ARL13B normais. Esta descoberta sugere que o papel da proteína não é apenas cronometrar o crescimento dos cílios, mas também ajudá-los a permanecerem sincronizados. “Nossa análise genética mostra que o ARL-13 afeta o alongamento cílios-cílios opostos, independente do comprimento dos cílios”, disse o Dr. Kaplan.
Os cientistas também descobriram que a interrupção de um grupo de proteínas acessórias chamado complexo proteico da síndrome de Bardet-Biedl – um grupo de proteínas que auxiliam no transporte de materiais dentro dos cílios – na verdade melhorou os problemas de alinhamento em vermes sem ARL13B. Isto sugere uma possível ligação entre os efeitos do ARL13B e alterações na camada externa dos cílios, chamada membrana ciliar, que atua como a pele que envolve a estrutura. “Acreditamos que o ARL-13 contribui para o alongamento aposicional dos cílios-cílios, em parte regulando a membrana ciliar”, explica o Dr.
A introdução da proteína ARL13B em C. elegans restaura o arranjo correto dos pares ciliares. Isto confirma a importância desta proteína única na manutenção da coordenação ciliar. A equipe também testou outros genes conhecidos por afetar o tempo de crescimento dos cílios, como a quinase tipo 1 dependente de ciclina, um gene envolvido na regulação da atividade celular, e a proteína 5 defeituosa que preenche o corante, que desempenha um papel na construção dos cílios. No entanto, estes genes não tiveram efeito no problema de alinhamento, sugerindo que diferentes vias biológicas controlam o comprimento ciliar e o crescimento lado a lado.
Algumas combinações de alterações genéticas causaram problemas mais óbvios. A remoção do ARL13B e de outro gene, o nephron2 (um gene associado à doença renal que também afeta os cílios), piorou o alinhamento. Quando um terceiro gene, a histona desacetilase 6, que ajuda a regular as proteínas e a estrutura celular, também foi removido, os cílios tornaram-se mais longos, mas ainda assim não conseguiram se alinhar. Estes resultados indicam que o ARL13B faz parte de uma rede proteica mais ampla que ajuda a manter a disposição correta dos cílios.
Para saber mais sobre o papel da superfície externa dos cílios, os cientistas estudaram substâncias específicas semelhantes à gordura, chamadas marcadores lipídicos, que normalmente estão localizadas na parte externa dos cílios. Na ausência de ARL13B, esta substância aparece no interior dos cílios, sinalizando alterações no comportamento da membrana. Quando o complexo proteico da síndrome de Bardet-Biedl foi removido desses mutantes, esse lipídio retornou à sua localização habitual, apoiando a ideia de que o ARL13B ajuda a controlar as membranas ciliares.
As descobertas do Dr. Kaplan e colegas fornecem um forte apoio à ideia de que o ARL13B ajuda a organizar os cílios, alterando sua superfície e não apenas sua estrutura interna. Dr. Kaplan acredita que outras moléculas pegajosas, chamadas moléculas de adesão, que ajudam as células a se ligarem umas às outras também podem ajudar a manter a forte associação entre esses pares de cílios e devem ser exploradas em estudos futuros.
Referência do diário
Turan MG, Kantarci H., Cevik S., Kaplan OI “ARL13B regula o alongamento cílios-cílios opostos de maneira dependente do complexo proteico da síndrome de Bardet-Biedl em Caenorhabditis elegans.” iScience, 2025. DOI: https://doi.org/10.1016/j.isci.2025.111791
Sobre o autor
Dra.Sebiha Sevik é bióloga molecular e investigadora principal da Universidade Abdullah Gul, na Turquia, onde se concentra nos mecanismos celulares por trás de doenças genéticas raras. O seu trabalho explora como as estruturas celulares, como os cílios, contribuem para a saúde e o desenvolvimento humano, com foco particular no seu papel na função sensorial e nas doenças. Dr. Cevik é autor de vários estudos influentes na área e orienta ativamente jovens cientistas em pesquisas biomédicas.

Dr. é geneticista da Universidade Abdullah Gul, conhecido por suas pesquisas sobre biologia ciliar e organização celular. Sua pesquisa investiga como os sinais moleculares coordenam o desenvolvimento e a estrutura das projeções celulares microscópicas, avançando nossa compreensão das doenças genéticas associadas à disfunção ciliar. Kaplan também é reconhecido por construir imagens inovadoras e ferramentas genéticas para estudar organismos modelo vivos, por ex. Caenorhabditis elegans.